據吉利德方面介紹,吉利德正在美國、亞洲和歐洲的新型冠狀病毒肺炎高發地區進行兩項三期研究。其中一項研究針對重症患者,另一項研究針對中症患者。這些研究要回答的眾多問題之一是治療時間是否可以從10天縮短到5天。
“重症的入組患者人數已達到了最初設計要求的人數,我們現在已經擴大了研究范圍,讓包括接受機械通氣的患者在內的更多患者可以參與其中。”Daniel O’Day在10日發布的公開信中提到。
此外,美國國家過敏和傳染病研究所(NIAID)於2月21日開始了一項全球試驗。該試驗將隨機分配患者使用瑞德西韋或安慰劑,以對照比較試驗結果。該試驗正在入組約800名具有不同症狀的患者。
在審批方面,今年3月,美國食品藥品監督管理局(FDA)公告稱,批准了針對治療新冠潛在有效藥物瑞德西韋的孤兒藥認証,適應症為新型冠狀病毒肺炎(COVID-19)。
不過,此事引發了不少爭議,一些業內人士擔心,孤兒藥資格可能會影響瑞德西韋的可及性。
隨后,吉利德發布聲明宣布已經向FDA提出申請,要求FDA撤銷瑞德西韋的孤兒藥資格認証,並放棄與孤兒藥資格相關的所有權益。
另一方面,吉利德方面已經迫不及待擴大產能。
Daniel O’Day本月4日曾發表公開信強調,已將瑞德西韋的生產全程時間從大約一年減少到約六個月。
他還強調,吉利德正力爭到10月份生產超過可供50萬個療程使用的藥品,到今年年底的可供應量要超過100萬個療程。
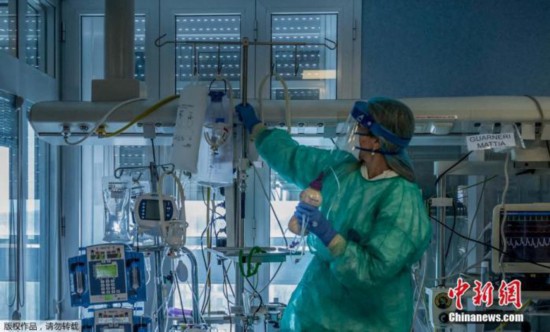
資料圖:當地時間3月23日,意大利米蘭東南部的克雷莫納醫院重症監護室,醫護人員正在為感染新冠狀肺炎的重症患者治療。
全球加緊尋求有效治療方法
如今,新冠肺炎疫情在全球蔓延態勢依舊嚴峻。
美國約翰斯·霍普金斯大學實時統計數據顯示,截至北京時間4月11日17時45分,全球新冠肺炎確診病例超過170萬例,死亡病例超10萬例。
除了被寄予厚望的瑞德西韋,目前,其他藥物的研發與試驗也在推進中。
美國國家衛生研究院(NIH)9日宣布啟動一項針對抗瘧疾藥——羥氯喹的臨床試驗。這項評測旨在研究其治療新冠肺炎患者的安全性和有效性。
研究由NIH下屬的國家心肺血液研究所(NHLBI)進行,首批參與臨床試驗的患者正在美國田納西州范德堡大學醫學中心登記。
據報道,FDA日前發布一份緊急使用授權,允許美國醫療服務人員將抗瘧疾藥物羥氯喹和氯喹用於治療新冠肺炎患者。雖然尚未掌握臨床証據証明該藥能安全有效地治療新冠患者,但是美國總統特朗普日前在白宮新聞發布會上堅決支持將該藥作為治療新冠肺炎患者的一種方法。
9日,俄羅斯衛生部推出6種藥物治療新冠肺炎,還有3種處於臨床試驗階段。這些藥物包括氯喹、羥氯喹、洛匹那韋+利托那韋、阿奇霉素(與羥氯喹配合使用)和干擾素藥劑。
與此同時,世衛組織與合作伙伴日前也發起了“團結”臨床試驗,這項國際臨床試驗旨在幫助找到有效治療新冠肺炎的方法。
據悉,“團結”臨床試驗將四種治療方案與標准護理進行比較,以評估它們對治療新冠肺炎的相對有效性。基於實驗室、動物和臨床研究証據,“團結”臨床試驗選擇了以下治療方案:瑞德西韋、洛匹那韋�利托那韋、洛匹那韋�利托那韋和干擾素β-1a、氯喹或羥氯喹。
“團結”臨床試驗在多個國家招募患者,目的在於快速發現是否有任何藥物能夠減緩疾病進展或提高存活率。根據新出現的証據,其他藥物也可能加入該試驗。(完)
(責編:馬曉波、張鑫)

